Alle Pflanzen vermitteln ihre Interaktionen mit der Umwelt über chemische Signale. Ein Beispiel dafür ist das Alkaloid Gramin, das von Gerste, einer der weltweit am häufigsten angebauten Getreidearten, produziert wird. Gramin bietet Schutz vor pflanzenfressenden Insekten und Weidetieren und hemmt das Wachstum anderer Pflanzen. Trotz langjähriger Forschung war das Schlüsselgen für die Bildung von Gramin aber bislang nicht bekannt.
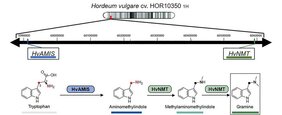
Die Forscherinnen und Forscher entdeckten in der Gerste nun ein Cluster von zwei Genen für die Gramin-Biosynthese. Das erste Gen (HvNMT) war bereits vor 18 Jahren gefunden worden. In ihrer Studie haben die Wissenschaftlerinnen und Wissenschaftler vom IPK und der Leibniz Universität Hannover jetzt ein zweites Schlüsselgen (AMI-Synthase, HvAMIS) für die Biosynthese identifiziert, das auf demselben Chromosom liegt. Damit ist jetzt der gesamte Stoffwechselweg von Gramin beschrieben.
„Wir haben entdeckt, dass AMIS ein Oxidase-Enzym ist, das eine ungewöhnliche kryptische oxidative Umlagerung von Tryptophan durchführt. Damit können wir die bisherige Theorie zur Gramin-Biosynthese aus den 1960er Jahren revidieren", sagt Dr. John D'Auria, Leiter der IPK-Arbeitsgruppe „Metabolische Diversität“. Prof. Dr. Jakob Franke, Leiter der Arbeitsgruppe „Biochemie sekundärer Pflanzenstoffe“ an der Leibniz Universität Hannover, ergänzt: „Der bisher unbekannte Enzym-Mechanismus, über den Gramin gebildet wird, hat uns sehr überrascht. Gleichzeitig bietet sich dadurch nun die Möglichkeit, biologisch aktive Alkaloide mit nachhaltigen biotechnologischen Methoden zu produzieren.“
Die Forscherinnen und Forscher konnten damit Gramin in Hefe und Modellpflanzen (Nicotiana benthamiana, Arabidopsis) herstellen. „Anders als bei vielen anderen pflanzlichen Abwehrstoffen sind zur Bildung von Gramin nur zwei Gene erforderlich. Dadurch lassen sich unsere Erkenntnisse relativ leicht praktisch nutzen“, hebt Ling Chuang von der Leibniz Universität Hannover, eine der Erstautoren, hervor. „Zudem ist es uns durch gentechnische Veränderung auch gelungen, Gramin in einer nicht graminproduzierenden Gerstensorte herzustellen und umgekehrt, die Graminproduktion in einer graminproduzierenden Gerstensorte durch Genom-Editierung zu unterbinden“, sagt Sara Leite Dias, ebenfalls Erstautorin der Studie und von der International Max Planck Research School geförderte Wissenschaftlerin am IPK.
„Die Ergebnisse ermöglichen die Herstellung von Gramin in Organismen, die eigentlich nicht die Fähigkeit haben, es selbst zu synthetisieren“, erklärt John D‘Auria. „Umgekehrt kann Gramin nun aus Gerste und anderen Gräsern eliminiert werden, um die Toxizität für Wiederkäuer zu verringern“, sagt der IPK-Wissenschaftler. „Unter dem Strich bilden die Ergebnisse die Grundlage für die Verbesserung der Gerste, um ihre Resistenz gegen Schädlinge künftig weiter zu erhöhen, ihre Toxizität für Wiederkäuer zu verringern und einen Beitrag zur nachhaltigen Unkrautbekämpfung zu leisten.“
(Leibniz-Institut für Pflanzengenetik und Kulturpflanzenforschung)
Originalpublikation:
Leite Dias et al. (2024): Biosynthesis of the allelopathic alkaloid gramine in barley by a cryptic oxidative rearrangement. Science. DOI: 10.1126/science.adk6112