Die Ergebnisse erweitern grundlegend das Wissen über PET-abbauende Enzyme, den zugrundeliegenden Mechanismus sowie das evolutionäre Verständnis über die Vielfalt mutmaßlicher PET-abbauender Enzyme im gesamten globalen Ozean. Das Forschungsteam veröffentlichte die Ergebnisse kürzlich im Fachjournal Communications Chemistry und diskutierte dabei sowohl biotechnologische Anwendungen als auch die hohe Relevanz für biogeochemische Prozesse im Meer und an Land.
Die Studie verdeutlicht eine Besonderheit des PET-abbauenden Enzyms. „Wir haben in unserer Studie eine neue genetische Ressource aus Tiefseeorganismen aus dem Reich der Archaeen entdeckt“, sagt Professorin Ruth Schmitz-Streit, Leiterin der Arbeitsgruppe Molekularbiologie der Mikroorganismen vom Institut für Allgemeine Mikrobiologie (IfAM) und Mitglied im CAU-Forschungsschwerpunkt Kiel Marine Science (KMS). Bisher bekannt waren etwa 80 verschiedene PET-abbauenden Enzyme, die überwiegend in Bakterien oder Pilzen gefunden wurden. „Unsere Daten tragen dazu bei, das Wissen über die ökologische Rolle der Tiefsee-Archaeen und die mögliche Zersetzung von PET-Abfällen im Meer zu erweitern“, so die Mikrobiologin.
Das neue Enzym: PET46
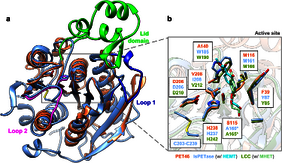
Das Forschungsteam hat erstmals das PET-abbauende Enzym PET46 aus einem nicht-kultivierten Tiefsee-Mikroorganismus mit einem metagenomischen Ansatz identifiziert und biochemisch beschrieben. Dazu wurde das Gen aus einer Tiefseeprobe anhand von Ähnlichkeiten zu bekannten Sequenzen identifiziert, das entsprechend kodierende Gen synthetisiert, das Protein in dem Bakterium Escherichia coli hergestellt und anschließend biochemisch und strukturell untersucht. PET46 besitzt viele ungewöhnliche Eigenschaften und erweitert den bekannten Bestand PET-abbauender Enzyme um einen fundamental neuen Bauplan. Strukturell unterscheidet sich das Enzym deutlich von bisher entdeckten Enzymen. Dadurch besitzt es die Fähigkeit sowohl sehr langkettige PET-Moleküle, sogenannte Polymere, als auch kurzkettigere PET-Moleküle, sogenannte Oligomere, abzubauen, wodurch der Abbau kontinuierlich ablaufen kann.
PET46 verwendet dabei unter anderem einen völlig anderen Mechanismus zur Substratbindung im Vergleich zu den bisher bekannten PET-abbauenden Enzymen. Das Forschungsteam beschreibt einen ungewöhnlichen „Deckel“ aus 45 Aminosäuren oberhalb des aktiven Enzymzentrums als entscheidend für die Bindung. Bei anderen PET Enzymen sind aromatische Aminosäuren nahe des aktiven Zentrums typisch.
Vielversprechende Anwendungen in der Biotechnologie
Auf molekularer Ebene weist PET46 große Ähnlichkeiten zu einem anderen Enzym, der Ferulasäure-Esterase, auf. Dieses baut das natürliche Polymer Lignin in Pflanzenzellwänden ab, indem sie Lignin-Polymere spalten und so den Zucker aus verholzen Pflanzenteilen lösen. Lignin und PET haben viele strukturelle Ähnlichkeiten, so dass die PET-abbauenden Enzyme in der Natur z.B. für die Kompostierung von Holz im Waldboden wichtig sein können.
Die biochemischen Eigenschaften von PET46 machen es damit sowohl für Kunststoffe aus dem Meer und von Land als auch biotechnologisch zu einem sehr interessanten Enzym. Im Vergleich zu bisher am detailliertesten beschriebenen PET-abbauenden Enzymen aus Bakterien und aus Kompostanlagen ist PET46 bei 70 Grad Celsius effizienter als andere Referenzenzyme bei ihren jeweiligen Optimums-Temperaturen.
Christian-Albrechts-Universität zu Kiel
Originalpublikation:
Perez-Garcia, P., Chow, J., Costanzi, E., (…), Schmitz-Streit, R., and Streit, W. R. An archaeal lid-containing feruloyl esterase degrades polyethylene terephthalate. Commun Chem 6, 193 (2023). DOI: 10.1038/s42004-023-00998-z, https://www.nature.com/articles/s42004-023-00998-z