Eine gut eingestellte Alarmanlage löst erst dann aus, wenn tatsächlich jemand versucht, unbefugt ins Haus einzudringen. Die Kunst besteht darin, Fehlalarme zu vermeiden, aber eben dann auszulösen, wenn konkrete Gefahr besteht. „Genau dies gilt auch für das menschliche Immunsystem im Umgang mit Krankheitserregern wie Viren. Denn unnötige Alarmzustände bedeuten Stress, und Überreaktionen des Immunsystems sind für den Organismus gefährlich“, erklärt Dr. Konstantin Sparrer, Leiter einer BMBF-Nachwuchsgruppe am Institut für Molekulare Virologie der Ulmer Universitätsmedizin.
Gemeinsam mit Professorin Michaela Gack, Direktorin des Florida Research and Innovation Center der Cleveland Clinic in Port Saint Lucie, hat Sparrer eine Studie geleitet, die untersucht, wie die Zelle bemerkt, ob sie mit RNA-Viren infiziert ist; dazu gehören beispielsweise SARS-CoV-2 aber auch Grippe- oder Zikaviren. Denn im Falle einer Infektion muss das Immunsystem schnell und gezielt reagieren können. Eine Schlüsselrolle bei der Viruserkennung und dem Auslösen einer antiviralen Antwort spielen zelluläre Sensorproteine, die bei „Gefahr im Verzug“ über bestimmte Signalübertragungswege die Immunabwehr mobilisieren.
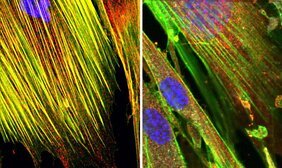
Doch wann werden diese Sensoren aktiv? Bislang wurde angenommen, dass bestimmte Moleküle – oft viralen Ursprungs – ausreichen, um eine Immunantwort auszulösen. Dazu gehören beispielsweise virale Genome oder auch virale Nukleinsäuren, die sozusagen am „falschen Ort“ sind. Das deutsch-amerikanische Forschungsteam – zu dem auch die beiden Leiter des Ulmer Instituts für Molekulare Virologie Professor Frank Kirchhoff und Professor Jan Münch gehören – fand nun heraus, dass allein die Präsenz dieser ‚fremden‘ Moleküle jedoch nicht ausreicht, damit Alarm geschlagen wird. Neu ist nun die Erkenntnis, dass es ein zweites Signal braucht, um Sensor-Proteine für RNA-Viren vollständig zu aktivieren. Treten diese Viren in Kontakt mit der Zelle oder vermehren sie sich in ihr, kommt es zu Strukturveränderungen im Aktin-Zytoskelett der Zelle. Diese minimalen Störungen der Ordnung werden von einem Protein (R12C) ausgelesen, das in der aktuellen Studie identifiziert wurde. Nur wenn beide Bedingungen erfüllt sind – die Präsenz von ‚fremden‘ Molekülen und eine Änderung des Zytoskeletts – werden die Sensorproteine aktiviert und eine vollständige Antwort des angeborenen Immunsystems ausgelöst. „Im Prinzip funktioniert das Zytoskelett einer Zelle hier wie das Netz einer Spinne. Es signalisiert bei Berührung, dass sich ein Eindringling nähert“, erläutert der Ulmer Virologe Sparrer.
„Die Bedeutung dieser Erkenntnis ist weitreichend. Sie erweitert die vorherrschende Lehrbuchmeinung um ein neues Konzept, wie das angeborene Immunsystem aktive Viren effektiv und selektiv erkennt. Dies kann sicherlich dabei helfen, antivirale Therapien und Impfstoffe noch effektiver zu machen“, so die deutsche Molekularbiologin Gack, die in Florida forscht. „Wir wissen jetzt auch mehr darüber, wie das Immunsystem Fehlalarme vermeidet“, ergänzen die Ulmer Forscher.
Universität Ulm
Originalpublikation:
Dhiraj Acharya, Rebecca Reis, Meta Volcic, GuanQun Liu, May K. Wang, Bing Shao Chia, Rayhane Nchioua, Rüdiger Groß, Jan Münch, Frank Kirchhoff, Konstantin M. J. Sparrer and Michaela U. Gack. Actin Cytoskeleton Remodeling Primes RIG-I-like Receptor Activation. In: Cell, September 15, 2022;
doi:10.1016/j.cell.2022.08.011, https://doi.org/10.1016/j.cell.2022.08.011