Allein innerhalb der Europäischen Union sind etwa drei Millionen Menschen von einer Autismus- Spektrum-Störung (ASS) betroffen. Bei manchen sind die Auswirkungen gering, so dass sie ein eigenständiges Leben führen können, andere haben schwere Behinderungen. Was die verschiedenen Formen gemeinsam haben, sind Schwierigkeiten sozial zu interagieren und zu kommunizieren sowie sich wiederholende, stereotype Verhaltensweisen. Mutationen in hunderten verschiedenen Genen werden mit ASS in Verbindung gebracht. Eines davon heißt Cullin 3 – ein Hochrisiko-Gen: Eine Mutation dieses Gens führt mit ziemlicher Sicherheit zu einer Form von ASS. Doch wie genau wirkt sich dieses Gen auf das Gehirn aus? Um mehr darüber zu erfahren, arbeiteten Jasmin Morandell und Lena Schwarz, Doktorandinnen in der Forschungsgruppe von Professor Gaia Novarino, mit Mäusen, deren Cullin 3-Gen teilweise ausgeschaltet wurde, und verglichen sie mit ihren gesunden Geschwistern. Ihre Ergebnisse wurden soeben im Fachmagazin Nature Communications veröffentlicht.
In einer Reihe von Verhaltens- und Bewegungstests wollte das Team herausfinden, ob die veränderten Mäuse Merkmale von Patient_innen mit dieser Form von Autismus nachvollziehen und somit als Modellorganismen verwendet werden können. In einem dieser Tests, dem sogenannten „Three Chamber Sociability Test“, konnte eine Maus drei benachbarte Kammern einer Box, die durch kleine Türen verbunden waren, erkunden. Anschließend setzten die Wissenschafter_innen zwei weitere Mäuse in die äußeren Boxen: Eine war der untersuchten Maus bereits vertraut, die andere hatte sie noch nie getroffen. "Gesunde Mäuse bevorzugen normalerweise die neue gegenüber der bereits bekannten Maus", erklärt Jasmin Morandell, Co-Erstautorin der Studie. Die Maus mit dem veränderten Cullin 3-Gen zeigte jedoch keine Anzeichen dafür. Außerdem hatten die Mäuse motorische Koordinationsdefizite sowie andere, für ASS typische, kognitive Beeinträchtigungen. Mit Hilfe dieses Mausmodells konnte das Team schließlich herausfinden, wie die beobachteten Veränderungen entstehen.
Gefährliche Ansammlung von Proteinen
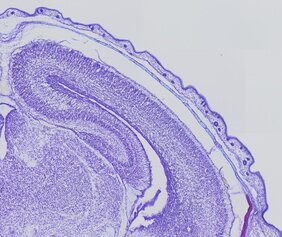
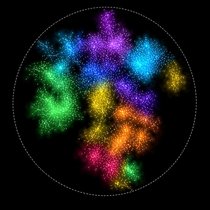
Als die Forschenden das Mäusegehirn untersuchten, fiel ihnen eine geringfügige, aber konstante Veränderung der Lage einiger Gehirnzellen auf. Diese so genannten Neuronen oder Nervenzellen entstehen in einer speziellen Region im Gehirn. Von dort wandern sie in Richtung der obersten Schichten, bis sie ihren vorgesehenen Platz in der Großhirnrinde erreichen. Dieser Prozess ist sehr sensibel – wandern die Zellen etwas zu langsam oder eine Spur zu schnell, verändert das die Zusammensetzung der Hirnrinde. Indem die Wissenschafter_innen die wandernden Neuronen markierten, konnten sie ihre Bewegungen nachvollziehen. "Wir konnten Migrationsdefizite beobachten – die Neuronen bleiben in den unteren Kortex-Schichten zurück", beschreibt Lena Schwarz, die zweite Co-Erstautorin der Studie. Aber warum bewegen sich die Zellen nicht so, wie sie sollten?
Die Antwort liegt in der wichtigen Rolle, die Cullin 3 am Lebensende von Proteinen spielt. Wenn ihre Zeit gekommen ist, markiert das Gen Cullin 3 sie für den Abbau – ein Prozess, der streng reguliert werden muss, damit sich die Proteine nicht anhäufen. Um herauszufinden, welche Proteine bei einem defekten Cullin 3-Gen fehlreguliert werden, analysierten Morandell und Schwarz systematisch die Proteinzusammensetzung des Mäusegehirns. "Wir haben Proteine untersucht, die sich im mutierten Gehirn anreichern und sind dabei auf ein Protein namens Plastin 3 aufmerksam geworden. Dann ist Gaia auf ein Poster über die Arbeit der Schur-Gruppe des IST Austria gestoßen – da wurde es dann richtig spannend", so Jasmin Morandell. "Sie hatten unabhängig von uns untersucht, wie Plastin 3 die Zellbeweglichkeit reguliert und dabei Ergebnisse erarbeitet, die unsere ergänzten, also haben wir begonnen, zusammenzuarbeiten", erinnert sich Professor Gaia Novarino.
Es stellte sich heraus, dass das Protein Plastin 3, das im Zusammenhang mit der neuronalen Zellmigration bisher unbekannt war, tatsächlich eine entscheidende Rolle in diesem Prozess spielt. "Wenn das Cullin 3-Gen deaktiviert ist, sammelt sich das Plastin 3-Protein an, was dazu führt, dass die Zellen langsamer und über kürzere Strecken wandern. Das ist genau das, was wir in der Großhirnrinde der modifizierten Cullin 3 Mäuse beobachten konnten", erzählt PhD-Studentin Lena Schwarz.
Ein kritisches Zeitfenster
All das findet in einem sehr frühen Stadium der Gehirnentwicklung statt, etwa in der Mitte der Schwangerschaft – lange bevor jemand einen Unterschied beim Fötus bemerken würde. "Dieses kritische Zeitfenster während der Gehirnentwicklung zu bestimmen, könnte extrem wichtig sein, um die Behandlung von Patient_innen mit bestimmten Formen von ASS zu verfeinern", erklärt Novarino, die sich dafür einsetzt, ASS besser diagnostizieren und Menschen so besser behandeln zu können. "Die weitere Erforschung von Plastin 3 könnte den Weg für neue Therapeutika ebnen. Die Ansammlung dieses Proteins zu hemmen, könnte eventuell einige der Symptome lindern, die die Patient_innen haben", sagt Schwarz.
"Wir wissen jetzt, dass ein defektes Cullin 3-Gen zu einem erhöhten Plastin 3-Spiegel führt. Diese enge Verbindung zeigt, dass der Plastin 3-Spiegel ein wichtiger Faktor dafür sein könnte, die Bewegung der Zellen zu kontrollieren", sagt Jasmin Morandell, die vor kurzem ihren Abschluss gemacht hat und ihr Fachwissen in Zukunft für die Erforschung der Huntington-Krankheit nutzen wird. Lena Schwarz wird sich nun am IST Austria weiteren ASS-Hochrisiko-Genen zuwenden, um zu sehen, wie der Abbau anderer Proteine mit ASS in Verbindung stehen könnte. Für die vorliegende Studie hat sich die Novarino-Gruppe mit der Danzl und der Schur Gruppe sowie einem Kollegen der Universität Rom zusammengetan. "Diese umfangreiche Studie trotz der Pandemie in rund zweieinhalb Jahren fertigzustellen, war nur mit der Unterstützung unserer Nachbarn am IST Austria möglich", lobt Novarino die Multidisziplinarität am Institut.
IST Austria
Originalpublikation:
Jasmin Morandell, Lena A. Schwarz et al. 2021. Cul3 regulates cytoskeleton protein homeostasis and cell migration during a critical window of brain development. Nature Communications. DOI: 10.1038/s41467-021-23123-x