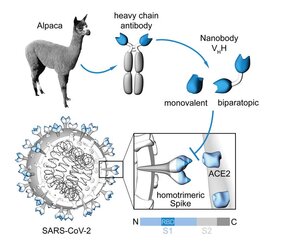
Nanobodies – kleine Helfer mit großem Potenzial
Nanobodies leiten sich von Einzeldomänen-Antikörpern ab, wie sie in Alpakas oder Dromedaren vorkommen. Grundsätzlich verhalten sich Nanobodies ähnlich wie herkömmliche Antikörper, sie haben jedoch entscheidende Vorteile. „Nanobodies sind deutlich kleiner und stabiler als Antikörper. Darüber hinaus lassen sie sich einfach und kostengünstig herstellen,“ beschreibt Prof. Rothbauer die Vorzüge. Die NMI-Forscherinnen und -Forscher gewinnen die Nanobodies aus den B-Lymphozyten immunisierter Alpakas. Nach Übertragung der Nanobody-DNA in Bakterien lassen sich die kleinen Bindungsmoleküle schnell und effizient im Labor produzieren.
In der Studie wurden Nanobodies entwickelt, die unterschiedliche Bereiche innerhalb der Rezeptorbindedomäne (RBD) von SARS-CoV-2 erkennen. Die RBD ist ein Teil des Spike-Proteins, welches auf der Oberfläche des SARS-CoV-2-Virus sitzt. Sie spielt eine besondere Rolle, da die RBD vom Virus genutzt wird, um an menschliche Zellen anzudocken und in die Zelle einzudringen. Die schützenden, neutralisierenden Antikörper, wie sie nach einer Infektion oder Impfung gebildet werden, richten sich ebenfalls gegen genau diese virale Struktur. „Das Ziel unserer Untersuchung war es, einen Test zu entwickeln, mit dem man einfach und schnell bestimmen kann, ob eine Person nach Infektion mit SARS-CoV-2 neutralisierende Antikörper gebildet hat,“ erklärt Teresa Wagner, Wissenschaftlerin in der Gruppe Rekombinante Antikörpertechnologien am NMI und Erstautorin der Studie.
Nanobodies im Einsatz
Nach der Auswahl der zwei bindungsstärksten Nanobodies, die an verschiedene Bereiche der RBD binden, wurden diese miteinander verbunden und in einen kompetitiven serologischen Bindungstest integriert, dem NeutrobodyPlex. Durch die gezielte Verdrängung mit dem Nanobody, kann man die Menge neutralisierender Antikörper aus Serumproben infizierter oder geimpfter Personen bestimmen. Im Vergleich zu herkömmlichen Antikörpertests ermöglicht der NeutrobodyPlex eine detaillierte Klassifizierung der neutralisierenden Antikörpermenge. Damit lässt sich beispielsweise überprüfen, ob eine infizierte Person Antikörper gebildet hat, die vor einer erneuten Infektion schützen, aber auch der Erfolg einer Impfung lässt sich beurteilen. „Die indirekte Messung der Antikörpermenge liefert schnell Ergebnisse in einer Vielzahl von Proben und es werden nicht wie bisher Labore der Sicherheitsstufe S3 für einen viralen Neutralisationstest benötigt“, erklärt Prof. Rothbauer. Eingesetzt wird der patentierte Bindungstest nun im Labor von Dr. Nicole Schneiderhan-Marra, Leiterin der Gruppe Multiplexe Immunoassays am NMI. Gleichzeitig kommt der NeutrobodyPlex bereits bei Serumanalysen zum Einsatz, die vom Zentrum für klinische Transfusionsmedizin in Tübingen durchgeführt werden. Blutproben von Patienten und geimpften Personen könnten dort untersucht werden.
Ermöglicht wurde die Entwicklung des NeutrobodyPlexT durch die schnelle Förderung des Ministeriums für Wirtschaft, Arbeit und Wohnungsbau Baden-Württemberg.
NMI Naturwissenschaftliches und Medizinisches Institut an der Universität Tübingen
Originalpublikation:
Wagner et al. (2021). NeutrobodyPlex - Nanobodies to monitor a SARS-CoV-2 neutralizing immune response. EMBO Reports