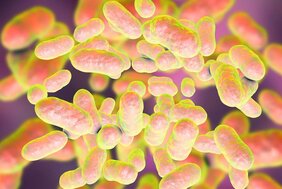
Das Darmmikrobiom ist ein hochkomplexes Ökosystem mit Tausenden unterschiedlicher Bakterienarten. Leben und leben lassen, das ist die Devise. Das harmonische Miteinander basiert darauf, dass die Darmbakterien unterschiedliche Nischen besetzen. Und es basiert darauf, dass die verschiedenen Bakterien miteinander kommunizieren.
Wann gewinnt Segatella die Oberhand?
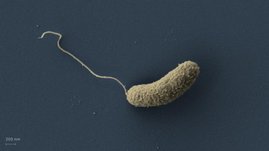
Die Zusammensetzung des Darmmikrobioms ist nicht immer gleich. Zwischen verschiedenen Regionen der Erde gibt es deutliche Unterschiede, in der westlichen hochindustrialisierten Welt etwa sind andere Bakterien vorherrschend als in Entwicklungsländern. Andererseits variiert das Darmmikrobiom – hinsichtlich vertretener Bakterienarten und deren Besiedelungsdichte – von Mensch zu Mensch. Trotz dieser Unterschiede gibt es grundlegende Muster der Darmbesiedelung, bei denen jeweils ein bestimmter Leitkeim dominiert. Bei einem dieser drei sogenannten Enterotypen ist Segatella copri der prominenteste Keim. Vor allem in Entwicklungs- und Schwellenländern kommt dieses Darmbakterium sehr häufig vor.
Trotz seiner weltweiten Verbreitung ist Segatella copri bisher nur wenig erforscht. Bekannt ist, dass sich das Bakterium auf den Abbau von Ballaststoffen spezialisiert hat. Unklar ist dagegen, welche Rolle es mit Blick auf die menschliche Gesundheit spielt: Ist es vorteilhaft oder hat es im Gegenteil negative Auswirkungen? Trotz der Fülle an Daten über das Mikrobiom geben bisherige Studien auf diese Frage keine Antwort.
Die gesundheitliche Bedeutung von Segatella copri aufzuklären, ist eines der Ziele der Forschungsarbeiten von Prof. Till Strowig, Leiter der Abteilung „Mikrobielle Immunregulation“ am HZI. Die Anzüchtung von Segatellen im Labor ist schwierig, aber Strowigs Arbeitsgruppe ist es doch gelungen. „Wir wollten herausfinden, unter welchen Bedingungen eine verstärkte Besiedelung mit Segatella copri stattfindet, und welche Prozesse dabei in den Zellen ablaufen. Dafür benötigen wir Einblicke in die Funktionsweise dieser Bakterien“, so Till Strowig.
Kleiner Schnipsel mit großer Wirkung
Das Programm für alle Lebensvorgänge ist in den Genen verschlüsselt aufgeschrieben. Das ist bei Bakterien nicht anders als beim Menschen. Wenn sich Segatella copri vermehrt und ausbreitet, werden komplexe Stoffwechselvorgänge in Gang gesetzt. Dafür müssen die zuständigen Gene abgelesen werden. Für diese Transkription wird die Erbinformation umgeschrieben, und zwar von DNA (Desoxyribonukleinsäure) in RNA (Ribonukleinsäure).
Welche Gene gerade aktiv sind, erfährt man durch Untersuchung des so genannten Transkriptoms. Das ist die Gesamtheit aller RNA-Moleküle, die zu einem bestimmten Zeitpunkt in einer Zelle vorhanden sind. „Bei der Untersuchung des Transkriptoms von Segatella copri sind wir auf einen winzigen RNA-Schnipsel gestoßen, der offenbar bei der Vermehrung und Ausbreitung des Bakteriums eine essenzielle Rolle spielt“ berichtet Erstautor Dr. Youssef El-Mouali. Das kleine Stückchen RNA – small RNA, so der Fachbegriff – ist maßgeblich beteiligt, wenn Segatella copri Neuland besiedelt. Das konnten die Forscher an Mäusen mit definiertem Darmmikrobiom zeigen. Dass „small RNAs“ bei der Regulation zellulärer Prozesse als wichtige Steuerelemente fungieren, ist auch von anderen Lebewesen einschließlich des Menschen bekannt.
Darmbakterien kommunizieren miteinander
Den bei Segatella copri entdeckten RNA-Schnipsel nannten die Forscher SrcF (Segatella RNA colonization factor) und nahmen ihn genauer unter die Lupe. Eine Frage, die sie klären wollten: Wann wird SrcF in den Zellen exprimiert? Die Vermutung liegt nahe, dass die Vermehrung des Bakteriums vom Nahrungsangebot abhängig ist. Bei einem hohen Angebot an Ballaststoffen, aus denen S. copri Energie gewinnt, werden sich die Bakterien ausbreiten und neue Lebensräume erobern. Tatsächlich konnten die Forscher zeigen, dass die Bildung von SrcF durch bestimmte komplexe Kohlenhydrate getriggert wird. Eine hohe Konzentration an Fruktanen – Mehrfachzucker, die vor allem aus Fruchtzucker (Fruktose) bestehen – unterdrückt dagegen die SrcF-Aktivität.
Und noch etwas fanden die Forscher heraus: Die Zusammensetzung des Mikrobioms hat einen Einfluss darauf, ob Segatella copri den Signalweg über SrcF aktiviert. Die vielen unterschiedlichen Bakterienspezies, die im Darm in friedlicher Koexistenz leben und um vorhandene Ressourcen konkurrieren, kommunizieren miteinander. Nur so ist der ausbalancierte Zustand des Mikrobioms zu erklären: Die individuelle Zusammensetzung des Darmmikrobioms ist erstaunlich konstant, und selbst nach vorübergehenden Turbulenzen stellt sich meist die alte Balance innerhalb dieses Ökosystems wieder her.
„Laut unseren Forschungsergebnissen scheint der Abbau größerer Mengen an Fruktanen die Kommunikation zwischen verschiedenen Darmbakterien zu beeinflussen“, so Till Strowig. „Wir werden weiter in diese Richtung forschen und hoffen, dass man das bessere Verständnis des Darmmikrobioms, zu dem wir beitragen möchten, irgendwann gezielt mit Blick auf die menschliche Gesundheit wird nutzen können.“
Helmholtz-Zentrum für Infektionsforschung
Originalpublikation:
El Mouali, Y., Tawk, C., Huang, K.D., Amend, L., Lesker, T.R., Ponath, F., Vogel, J., Strowig, T., The RNA landscape of the human commensal Segatella copri reveals a small RNA essential for gut colonization, Cell Host & Microbe (2024). https://doi.org/10.1016/j.chom.2024.09.008