Wird die Kinase blockiert, verringert sich die Virusproduktion
Mittels Live-Cell-Mikroskopie, quantitativer Immunfluoreszenz und biochemischen Analysen konnten die Forschenden zeigen, dass JNK gezielt in infizierten Zellen aktiviert wird. Mit einem sogenannten Kinase Translocation Reporter (KTR) machten sie direkt sichtbar, dass die JNK-Aktivität rund 16 Stunden nach der Infektion stark zunimmt. Wird die Kinase mit spezifischen Inhibitoren blockiert, verringert sich die Virusproduktion signifikant – sowohl bei HCoV-229E als auch bei SARS-CoV-2.
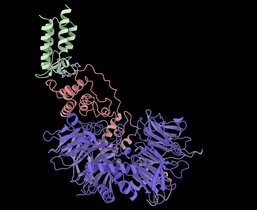
In Zusammenarbeit mit der Arbeitsgruppe von Prof. Dr. Michael Kracht an der Universität Gießen konnte das Team außerdem zeigen, dass JNK bestimmte Serin-Reste am N-Protein phosphoryliert. Diese Stellen sind bei verschiedenen Coronaviren konserviert, was darauf hindeutet, dass JNK eine gemeinsame Rolle in der Replikation unterschiedlicher Virustypen spielt. „Unsere Daten heben die JNK-Kinase als wichtigen Wirtfaktor hervor, der direkt an der Modifikation des N-Proteins beteiligt ist – ein für die Viren kritischer Schritt in der Vermehrung“, erklärt Yannick Brüggemann. Eike Steinmann ergänzt: „Dass die Inhibition von JNK die Vermehrung sowohl von HCoV-229E als auch von SARS-CoV-2 hemmt, unterstreicht das Potenzial dieses Signalwegs, künftig als Ausgangspunkt für neue antivirale Wirkstoffe.“
(Ruhr-Universität Bochum)
Originalpublikation:
Yannik Brüggemann et al.: JNK kinase regulates phosphorylation of HCoV-229E nucleocapsid protein, in: npj Viruses, 2025, DOI: 10.1038/s44298-025-00152-7, https://www.nature.com/articles/s44298-025-00152-7