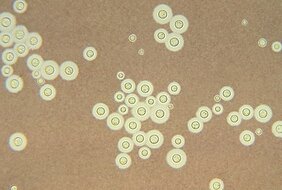
Hefepilze spielen eine große Rolle im Leben von uns Menschen. Sie geben uns zu essen, vom herzhaften Pizzateig bis zum süßen Hefezopf, sie ermöglichen es uns, Bier zu brauen, Wein zu keltern oder helfen uns im Kampf gegen Krankheiten als wichtiger Bestandteil von Medikamenten.
Und sie können uns umbringen.
Wie zum Beispiel Cryptococcus neoformans. Der weit verbreitete Hefepilz kommt unter anderem in Vogelmist vor und gelangt über die Atmung in den menschlichen Körper. „Für gesunde Menschen ist das kein Problem. Hier richtet Cryptococcus keinen Schaden an“, berichtet Karin Römisch, Professorin für Mikrobiologie an der Universität des Saarlandes. „Bei immungeschwächten Menschen jedoch kann Cryptococcus schwere Krankheiten auslösen, zum Beispiel eine Hirnhautentzündung“, erklärt die Expertin. Insbesondere HIV-Patienten sterben häufig an den Folgeerkrankungen nach Cryptococcus-Infektion. Von einer Million Erkrankten im Jahr sterben rund 700.000, berichtet die Biologin. Problematisch ist das insbesondere in wärmeren Weltregionen mit einem hohen Anteil von HIV-Infizierten, beispielsweise im Subsahara-Afrika.
Karin Römisch hat nun eine Studie veröffentlicht, in der sie gemeinsam mit Kolleginnen und Kollegen zeigt, wie man Cryptococcus neoformans unschädlich machen kann. Bildlich gesprochen: Sie montieren den Türgriff der Tür ab, durch die die krankheitserregenden Bestandteile der Hefezelle ihren Weg ins menschliche Gewebe nehmen. Der Türgriff ist dabei ein Protein namens Sbh1. Diese Eiweißstruktur ist Teil des Eintritts-Kanals in den „sekretorischen Weg“, der Weg vom Zellinneren zur Zelloberfläche und den extrazellulären Raum. In Hefen wie Cryptococcus neoformans werden bestimmte Enzyme, Melanin-Körnchen und eine Kapsel aus Zuckerpolymeren durch diesen „sekretorischen Weg“ zur Zelloberfläche transportiert. Diese drei Faktoren sind notwendig, damit Cryptococcus in den immungeschwächten Befallenen wachsen und die schweren Krankheiten auslösen kann.
Römisch und ihre Kolleginnen und Kollegen haben nun die Hefe genetisch so verändert, dass sie Sbh1 nicht mehr herstellen kann, also „der Türgriff abmontiert“ wird, um im Bild zu bleiben. Die krankheitsauslösenden Enzyme, Melanin-Körnchen und die Kapsel gelangen nicht mehr an die Hefeoberfläche und ins menschliche Gewebe. In der Folge konnten die Wissenschaftlerinnen und Wissenschaftler um Karin Römisch eine wegweisende Beobachtung machen: „Unter Infektionsbedingungen, bei 37 Grad Celsius, wie sie im menschlichen Körper herrschen, war die genetisch modifizierte Hefe ohne Sbh1 komplett harmlos.“
Karin Römisch und ihr Team haben die Menge der unveränderten Wildtyp-Hefe mit Sbh1 und der genetisch veränderten Zellen ohne Sbh1 im Lungen- und Hirngewebe von infizierten Mäusen gemessen; an diesen Stellen lösen sie im menschlichen Körper schwere Krankheiten aus. Das Ergebnis hätte nicht eindeutiger sein können: „Die Mutante hat sich in keinem Fall weiter vermehrt und die Tiere blieben gesund, während sich der Wildtyp in den Tieren stark vermehrt hat und zur Erkrankung der Tiere führte“, so die Wissenschaftlerin. „Cryptococcus neoformans ohne Sbh1 ist damit komplett avirulent“, sagt Karin Römisch.
Die Erkenntnisse aus dieser Studie sind umso bedeutender, wenn man zweierlei Probleme bedenkt, die miteinander zusammenhängen. Erstens gibt es gegen wenige Hefe-Infektionen wirksame Medikamente. Das hängt mit Problem Nummer zwei zusammen: Hefezellen ähneln im Aufbau sehr stark menschlichen Zellen. Man läuft also schnell Gefahr, dass ein Wirkstoff nicht nur die schädlichen Hefen angreift, sondern auch die umliegenden menschlichen Zellen. Der Versuch, ein wirksames Medikament gegen einen Hefepilz zu finden, ähnelt also in gewisser Weise dem Versuch, ein nasses Stück Seife in der Dusche aufzuheben: Es gibt kaum gute Angriffspunkte. „Das Protein Sbh1 ist nun eines der ganz wenigen spezifischen Targets in der Hefezelle , das wir angreifen können, da es beim Menschen anders aussieht. Das macht die Erkenntnis aus unseren Experimenten so bedeutsam“, erklärt Karin Römisch.
Ihre Hoffnung ist es, dass auf Basis ihrer Grundlagenforschung wirksame Medikamente gegen eine Cryptococcus-Infektion entwickelt werden könnten, um jedes Jahr hunderttausende Menschenleben zu retten.
Universität Saarland
Originalpublikation:
Felipe H. Santiago-Tirado, Thomas Hurtaux, Jennifer Geddes-McAlister, Duy Nguyen, Volkhard Helms, Tamara L. Doering, Karin Römisch: The ER protein translocation channel subunit Sbh1 controls virulence of Cryptococcus neoformans, mBio, https://doi.org/10.1128/mbio.03384-22