In einer Studie hat ein internationales Team unter der Leitung von Christian Gutt und Nimmi Das Anthuparambil von der Universität Siegen und vom DESY in Hamburg die physikalischen Prinzipien aufgedeckt, die die Bewegung von Lipoproteinen im Eigelbplasma, der durchsichtigen, flüssigen Komponente des Eigelbs, bestimmen. Mithilfe modernster Röntgentechnik am European XFEL beobachteten die Wissenschaftler:innen die Fett transportierenden Partikel im Mikrosekundenbereich – mit Aufnahmen, die über eine Million Mal schneller sind als ein Wimpernschlag.
Beobachtung bisher unsichtbarer Bewegungen
Aufgrund der extremen Dichte von Bestandteilen im Eigelb war es mit herkömmlichen Methoden nicht möglich, die Bewegung dieser Partikel zu erfassen. Um dieses Problem zu lösen, setzten die Forschenden die Megahertz-Röntgenphotonen-Korrelationsspektroskopie (x-ray photon correlation spectroscopy, MHz-XPCS) am European XFEL ein. „Die einzigartige Abfolge von Röntgenpulsen des European XFEL ermöglicht es uns, die Strukturdynamik im Mikrosekundenbereich zu untersuchen“, erklärt Anders Madsen, leitender Wissenschaftler und verantwortlich für das Instrument „Materials Imaging and Dynamics“ (MID) am European XFEL.
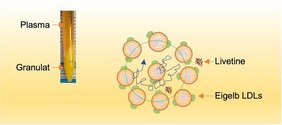
„MHz-XPCS erfasst diese schnellen, feinen Bewegungen in dicht gepackten biologischen Flüssigkeiten in Echtzeit – Dynamiken, die sonst verborgen bleiben.“ Zum ersten Mal beobachtete das Team direkt, wie sich die Fettpartikel bewegen, kollidieren und mit ihren Nachbarn interagieren. Die LDLs navigieren durch eine dicht gepackte Suspension aus anderen LDLs und löslichen Proteinen, genannt Livetine. Diese bilden temporäre „Käfige“ um die LDLs, die eine freie Diffusion verhindern.
Die LDLs werden gefangen, rütteln innerhalb dieser Begrenzungen und entkommen dann langsam. „Um die enorme Datenmenge zu bewältigen, die von MHz-XPCS generiert wird, ist eine Datenanalyse vor Ort während des Experiments erforderlich. Zusammen mit unseren Kollegen haben wir diese Herausforderung gemeistert, um diese Live-Informationen zu ermöglichen“, fügt Johannes Möller, Instrumentenwissenschaftler bei MID, hinzu.
Unerwartete Langsamkeit
Diese Eingrenzung verlangsamt die LDL-Bewegung dramatisch – um bis zu 100 Mal im Vergleich zu verdünnten Lösungen. Überraschenderweise verhält sich Eigelb trotz dieser Verlangsamung nicht wie ein festes Material, sondern wie eine dickflüssige, aber dennoch fließfähige Flüssigkeit. „Dieser träge Flüssigkeitszustand scheint genau das zu sein, was die Biologie braucht“, sagt die Erstautorin Nimmi Das Anthuparambil. „Er sorgt dafür, dass Nährstoffe sicher gespeichert bleiben und dennoch kontrolliert transportiert werden können, wenn der Embryo sie benötigt.“ Eine überraschende Erkenntnis ist, dass die LDL-Diffusion in dichtem Eigelb nicht dem üblichen Verhalten folgt.
Normalerweise verlangsamt sich die Diffusion vorhersehbar mit zunehmender Viskosität der Flüssigkeit, was durch die Stokes-Einstein-Beziehung beschrieben wird. In dieser gedrängten Umgebung bewegen sich weiche LDLs jedoch viel langsamer als erwartet, was auf einen Bruch dieses klassischen Gesetzes hindeutet. Die beobachtete Eingrenzung kann die Langsamkeit nicht vollständig erklären. „Das bedeutet, dass neue Modelle erforderlich sind, um den Transport in komplexen biologischen Flüssigkeiten zu verstehen“, erklärt der leitende Forscher Christian Gutt von der Universität Siegen. Die Forschenden konnten zeigen, dass die Verlangsamung nicht allein durch die Viskosität erklärt werden kann. Vielmehr spielen die Weichheit der Partikel und weitreichende hydrodynamische Wechselwirkungen eine entscheidende Rolle, sodass klassische Diffusionstheorien für harte Kugeln unter diesen beengten Bedingungen versagen.
Über Eigelb hinaus bedeutend
Das Verständnis der Bewegung von Partikeln in komplexen biologischen Flüssigkeiten hat Auswirkungen weit über die Embryonalentwicklung hinaus. Ähnliche dichte Umgebungen finden sich in lebenden Zellen, proteinreichen Lösungen und in Systemen zur Zufuhr von Medikamenten, die Lipoproteine als natürliche Nanotransporter verwenden.
Durch die Kombination von ultraschnellen Röntgenexperimenten mit einem neuen theoretischen Ansatz stellt diese Studie einen quantitativen Zusammenhang zwischen der mikroskopischen Struktur und dem großräumigen Transport in dichten Systemen aus weicher Materie her. Dieser Ansatz kann auf verschiedene biologische und technologische Materialien angewendet werden – vom Zellinneren bis hin zu pharmazeutischen Rezepturen. Lipoproteine niedriger Dichte sind vielversprechende natürliche Wirkstoffträger, und ihre Fähigkeit, sich in gedrängten Umgebungen effizient zu bewegen, hat direkten Einfluss auf ihre Wirksamkeit. „Das Leben hängt von der Bewegung in gedrängten Umgebungen ab – Moleküle und Partikel müssen sich unter Einschränkungen bewegen, ohne dass das System fest wird“, sagt Sakura Pascarelli, wissenschaftliche Direktorin bei European XFEL. „Studien wie diese zeigen, wie fortschrittliche Röntgenmethoden die Physik entschlüsseln können, die Leben möglich macht.“
European XFEL GmbH
Originalpublikation:
N.D. Anthuparambil et al.: Lipoprotein diffusion in dense yolk plasma is governed by softness, hydrodynamics, and caging: Insights from MHz-XPCS, Proc. Natl. Acad. Sci. U.S.A. 123 (8) e2519681123, https://doi.org/10.1073/pnas.2519681123 (2026).