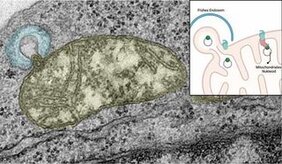
Mitochondrien sind die Kraftwerke unserer Zellen und haben aufgrund ihrer evolutionären Abstammung von Bakterien noch genetisches Material, verpackt in chromosomenähnliche Strukturen (Nukleoide). Sie wandeln die chemische Energie in unserer Nahrung in eine biologisch verwertbare Form um. In ihrer Arbeit zeigen die Forscher*innen, dass Mutationen der mtDNA zu einer lokalen Umlagerung von Proteinen in der Mitochondrienmembran führen. Die mutierte mtDNA wird so gezielt eliminiert und der Autophagie, der zellulären „Müllabfuhr“, zugeführt. An der Studie waren Forscher*innen des Zentrums für Physiologie der Medizinischen Fakultät der Universität zu Köln, des Zentrums für Molekulare Medizin (ZMMK) und des Exzellenzclusters für Alternsforschung CECAD beteiligt. Die Ergebnisse sind in dem Artikel „Mitochondrial membrane proteins and VPS35 orchestrate selective removal of mtDNA“ in Nature Communications veröffentlicht worden.
In vielen Geweben häufen sich Mutationen in der mtDNA als Folge des normalen Alterns an. Solche Mutationen sind dann eine wichtige Ursache für viele altersbedingte Krankheiten. mtDNA ist in Tausenden von Kopien pro Zelle vorhanden, so dass die mitochondriale Funktion nur dann beeinträchtigt ist, wenn der Prozentsatz der mutierten mtDNA-Moleküle einen Schwellenwert überschreitet. Schon lange ist bekannt, dass eine mitochondriale Schädigung, einschließlich einer akuten mtDNA-Schädigung, den Prozess der Mitophagie auslöst. Dabei werden dysfunktionale Mitochondrienteile gezielt abgebaut und recycelt.
Dr. David Pla-Martin, der Hauptautor der aktuellen Studie, erklärt die Details: „Neu in unserer Studie ist, dass dieser Mechanismus die Ausstattung der Zellen mit Mitochondrien nicht beeinträchtigt, sondern diese nur von geschädigter mtDNA gereinigt werden. Mit Hilfe von Markierung benachbarter Proteine – dem sogenannten Proximity Labelling - konnten wir zeigen, dass mtDNA-Schäden zur Rekrutierung von Endosomen in unmittelbarer Nähe zu Nukleoiden führen.“ Deren Entfernung wird durch die Interaktion des Nukleoid-Proteins Twinkle und den mitochondrialen Membranproteinen SAMM50 und ATAD3 koordiniert. ATAD3 steuert dabei ihre Verteilung, SAMM50 induziert die Freisetzung und den Transfer des Nukleoids zu den sogenannten Endosomen. „Dadurch wird zusätzlich die Aktivierung einer Immunantwort verhindert. Das Protein VPS35, die Hauptkomponente des Retromers, vermittelt die Reifung von frühen Endosomen zu späten Autophagie-Vesikeln, in denen der Abbau und das Recycling letztendlich stattfindet,“ so Pla-Martin.
Anhand eines Mausmodells, bei dem mtDNA-Mutationen zu einer Beeinträchtigung der Muskelregeneration führen, zeigten die Wissenschaftler*innen außerdem, dass selektiv mutierte mtDNA entfernt werden kann, indem die Aktivität der Autophagiemaschinerie durch Rapamycin stimuliert wird. Die Gesamtanzahl an mtDNA-Kopien bleibt so konstant, wodurch die mitochondriale Funktion erhalten bleibt.
Prof. Dr. Rudolf Wiesner, der Leiter der Gruppe, fügt hinzu: "Mutationen in den Genen, die für diese Proteine kodieren, führen zu schweren neurologischen Erkrankungen, bei VPS35 z.B. Parkinson. Wir wollen diese Proteine nun als neue molekulare Ziele nutzen, um ganz neue Behandlungsmöglichkeiten für solche altersbedingten Krankheiten zu eröffnen.“ Obwohl der Weg bis hin zur therapeutischen Anwendung noch lang sein könnte, sieht das Forschungsteam hier einen vielversprechenden Ansatz.
Universität Köln
Originalpublikation:
Sen, A., Kallabis, S., Gaedke, F. et al. Mitochondrial membrane proteins and VPS35 orchestrate selective removal of mtDNA. Nat Commun13, 6704 (2022). doi.org/10.1038/s41467-022-34205-9