Die meisten Medikamente wirken, indem sie ein Protein hemmen – sie blockieren seine Funktion, lassen das Protein selbst aber bestehen. Der gezielte Proteinabbau (englisch: targeted protein degradation) verfolgt einen anderen Ansatz: Er nutzt die Qualitätskontrolle der Zelle, um schädliche Proteine komplett abzubauen. Dazu bringen sogenannte „Degrader“-Moleküle ein Zielprotein in die Nähe einer E3-Ligase. Dieses Enzym markiert das Protein für den Abbau durch das zelluläre Recyclingsystem, das Proteasom. Besonders spannend ist dieser Ansatz, weil er auch Proteine angreifbar macht, die sich nur schwer direkt hemmen lassen. Und weil er nicht nur deren Aktivität, sondern auch ihre strukturelle Rolle in der Zelle ausschaltet.
Eine neue Ebene der Kontrolle
Bisher hatten die meisten dieser Wirkstoffe jedoch einen Haken: Sie nutzten jeweils nur eine einzige E3-Ligase. Fällt dieser Weg aus – etwa durch Mutationen oder Anpassungen von Krebszellen – kann das Medikament wirkungslos werden. Diese Schwachstelle zu überwinden, ist eine zentrale Herausforderung in der Forschung.
In ihrer aktuellen Studie untersuchten Forschende aus der Gruppe von Georg Winter am CeMM Forschungszentrum für Molekulare Medizin und AITHYRA – beides Institute der Österreichischen Akademie der Wissenschaften – gemeinsam mit dem Team von Alessio Ciulli am Centre for Targeted Protein Degradation (CeTPD) in in Dundee, Schottland, ein kleines Molekül, das auf die Proteine SMARCA2/4 abzielt. Diese spielen als zentrale Bestandteile eines Chromatin-Komplexes eine wichtige Rolle bei der Regulation von Genen und sind häufig an Krebs beteiligt.
Dabei machten die Forschenden eine überraschende Entdeckung: Das Molekül nutzt nicht nur eine, sondern gleich zwei verschiedene E3-Ligasen. Beide Wege können unabhängig voneinander den Abbau des Zielproteins auslösen, und erst wenn beide ausgeschaltet werden, stoppt der Abbauprozess vollständig.
Zwei Wege, ein Ziel
Dieses Prinzip funktioniert wie ein eingebautes Backup-System: Wenn ein Abbauweg blockiert ist, übernimmt der andere. Solche Redundanz ist in biologischen Systemen weit verbreitet, in der Wirkstoffentwicklung jedoch bislang selten. Er könnte entscheidend dazu beitragen, Therapien stabiler zu machen.
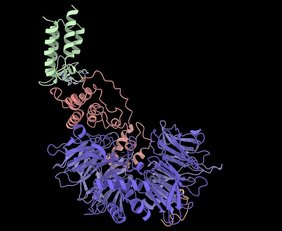
Wie genau dieser Mechanismus funktioniert, konnten die Forschenden mit einer Kombination aus genetischen, biophysikalischen und strukturellen Methoden aufklären. Das Molekül bringt das Zielprotein gezielt mit einer E3-Ligase zusammen und bildet einen hochspezifischen Komplex. Gleichzeitig kann es aber auch eine zweite Ligase rekrutieren und so einen alternativen Weg zum gleichen Ergebnis eröffnen.
Feinabstimmung der zellulären Entsorgung
Durch kleine chemische Veränderungen am Molekül können die Forscher beeinflussen, welche der beiden Ligasen bevorzugt genutzt wird. Auch minimale genetische Unterschiede in den Ligasen selbst spielen eine Rolle, wodurch sich die doppelte Rekrutierung gezielt steuern lässt.
„Wenn ein einzelnes Molekül mehrere Abbauwege gleichzeitig aktivieren kann, entsteht eine Art eingebaute Redundanz“, erklärt Georg Winter, korrespondierender Co-Autor der Studie, Life Science Director bei AITHYRA und Adjunct Principal Investigator am CeMM. „Das könnte helfen, eines der größten Probleme aktueller Degrader-Therapien zu überwinden – nämlich ihre Anfälligkeit für Resistenzen.“
„Das ist eine außerordentlich wichtige Entwicklung“, sagt Alessio Ciulli, ebenfalls korrespondierender Co-Autor der Studie und Direktor des CeTPD. „Die strukturellen Details, die wir hier gewinnen konnten, sind bemerkenswert. Wir können genau erkennen, wie dieses kleine Molekül einen neuen molekularen Handschlag zwischen Proteinen erzeugt, die normalerweise nicht miteinander interagieren würden. Da wir chemisch steuern können, welches Enzym die eigentliche Arbeit übernimmt, eröffnet sich für medizinische Chemiker:innen ein neuer Ansatz bei der Entwicklung der nächsten Generation von Krebsmedikamenten. Die Zusammenarbeit unserer beiden Gruppen hat sich erneut als starke Triebkraft für grundlegende wissenschaftliche Entdeckungen erwiesen.“
Die Bedeutung dieser Entdeckung reicht über ein einzelnes Zielprotein hinaus. Gerade in der Krebstherapie entstehen Resistenzen häufig dadurch, dass Zellen Wege finden, die Wirkmechanismen von Medikamenten zu umgehen. Wenn ein Wirkstoff jedoch mehrere Abbaupfade gleichzeitig nutzt, wird es für die Zelle deutlich schwieriger, sich anzupassen.
Insgesamt erweitert die Studie das Verständnis der gezielten Protein-Degradation grundlegend. Sie zeigt, dass zukünftige Medikamente nicht nur präzise, sondern auch besonders widerstandsfähig konzipiert werden könnten – und damit langfristig wirksamer bleiben.
CeMM Forschungszentrum für Molekulare Medizin der Österreichischen Akademie der Wissenschaften
Originalpublikation:
Spiteri, V.A., Segal, D., Correa-Sáez, A. et al. Dual E3 ligase recruitment by monovalent degraders for tunable SMARCA 2/4 degradation. Nat Chem Biol (2026). doi.org/10.1038/s41589-026-02224-y