DNA-Schäden, die repariert werden müssen, und Gene, die abgelesen werden sollen: für beide Prozesse ist das Enzym XPB, das Teil des TFIIH Komplexes ist, essentiell. Wie wichtig ein korrekt arbeitendes XPB ist zeigt, dass eine Fehlfunktion desselben zu den schweren Krankheiten Xeroderma Pigmentosum und Trichothiodystrophie führen kann.
Die Forschungsgruppe von Prof. Caroline Kisker vom Rudolf-Virchow-Zentrum – Center for Integrative and Translational Bioimaging der Universität Würzburg konnte nun zeigen, dass die TFIIH Untereinheiten p52/p8 die Funktionalität des Enzyms XPB kontrollieren, indem sie es einerseits aktivieren und andererseits dafür sorgen, dass es nicht zu schnell arbeitet. Diese Ergebnisse verbessern das Verständnis des Proteinkomplexes TFIIH und seiner wichtigen Funktionen.
Feinjustierung der Geschwindigkeit von XPB
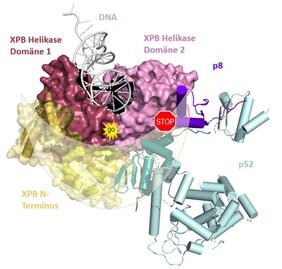
Während der Transkription bindet XPB an die Doppelhelix der DNA, wandert an ihr entlang und bewirkt somit, dass die beiden Stränge aufgetrennt werden, damit die Gene abgelesen werden können. Um das Enzym zu aktivieren, müssen die beiden Untereinheiten von XPB (im Bild rosa und rot) in enge räumliche Nähe zueinander gebracht werden. Diese Annäherung wird zum einen dadurch erreicht, dass p8/p52 an XPB bindet, oder, in noch stärkerem Ausmaß, wenn DNA gebunden wird. „Sind beide aktivierenden Faktoren simultan gebunden, würde man eigentlich vermuten, dass die stärkere Aktivierung sich durchsetzt, das Gegenteil ist aber der Fall“, sagt Dr. Jochen Kuper der als Postdoktorand in der Arbeitsgruppe forscht. „Mit unserer Struktur- und Funktionsanalyse konnten wir zeigen, dass durch p52/p8 die Beweglichkeit der Enzymuntereinheiten eingeschränkt wird. P52/p8 wirkt also wie eine Bremsbacke und verlangsamt die Geschwindigkeit von XPB“, erklärt Kisker. Dadurch wird sichergestellt, dass XPB korrekt arbeitet, denn während der Transkription und während der DNA Reparatur ist eine exakte Regulierung des Enzyms essentiell. In der vorgelegten Arbeit hat das Forscherteam nun p52/p8 als Masterregulatoren von XPB identifiziert. „Unsere Ergebnisse erklären auch, warum eine Mutation in so einer winzigen Untereinheit wie p8, so schwerwiegende Folgen haben kann, wie die Erkrankung an Trichothiodystrophie“, sagt Jeannette Kappenberger, Doktorandin in der Arbeitsgruppe Kisker und Erstautorin der Studie.
Die Wissenschaftlerinnen und Wissenschaftler planen nun weitere strukturelle und funktionale Untersuchungen der Proteine. Außerdem möchten sie herausfinden, wie der Komplex mittels Inhibitoren gezielt beeinflusst werden kann.
Rudolf-Virchow-Zentrum, Universität Würzburg
Originalpublikation:
Kappenberger J., Koelmel W., Schoenwetter E., Scheuer T., Woerner, J., Kuper J., Kisker C. How to limit the speed of a motor: The intricate regulation of the XPB ATPase and Translocase in TFIIH Nucleic Acids Research (November 2020) doi: 10.1093/nar/gkaa911