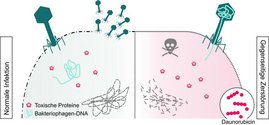
Eine neue Studie in der renommierten Fachzeitschrift Nature zeigt nun, dass menschliche Zellen dieser viralen Sabotage nicht hilflos ausgeliefert sind. Sie erkennen die Störung der Transkriptionstermination als Alarmsignal, aktivieren ein „Selbstzerstörungsprogramm“ und opfern sich selbst – noch bevor sich das Virus in ihnen vermehren kann. So gelingt es ihnen, die Ausbreitung der Infektion bereits im Keim zu ersticken. Dies sind die Forschungsergebnisse eines internationalen Teams aus Philadelphia (USA), Charlestown (USA), Chengdu (China) und Hannover.
Evolution hat virale Sabotage in Abwehr verwandelt
Das Forschungsteam fand heraus, dass die unnatürlich langen RNA-Moleküle eine besondere Struktur annehmen: Sie winden sich zu linksdrehenden Doppelsträngen, den sogenannten Z-RNAs. Diese ungewöhnlichen RNA-Formen werden vom zellulären Protein ZBP1 erkannt. Und dann startet der kontrollierte Zelltod. Besonders bemerkenswert ist, dass sich Z-RNAs vor allem in jenen Abschnitten dieser unnatürlich langen RNA-Moleküle bilden, die unter anderem von Überbleibseln früherer Virusinfektionen stammen. Diese ansonsten stillen Bereiche unseres Genoms werden nur aufgrund der virusbedingten Störung der Transkriptionstermination in RNA überschrieben.
„Unsere Zellen nutzen also ausgerechnet jene genetischen Überreste uralter Virusinfektionen, um aktuelle Virusangriffe zu erkennen und abzuwehren“, erklärt Prof. Lars Dölken, einer der vier korrespondierenden Autoren der Arbeit. Er leitet das Institut für Virologie der Medizinischen Hochschule Hannover (MHH) und ist designierter Kosprecher des Exzellenzclusters RESIST. Damit kehrt die Evolution den Spieß um: Was einst als virale Invasion begann, dient heute als Alarmsignal für die antivirale Immunabwehr. Diese Entdeckung zeigt eindrucksvoll, wie eng Virus und Wirt über Millionen Jahre miteinander verflochten sind – und wie unsere Zellen virale Sabotage in hochwirksame Schutzstrategien umwandeln können.
Neue Perspektiven für Therapien
Die Entdeckung hat weitreichende Bedeutung über Virusinfektionen hinaus. Unnatürlich lange RNA-Moleküle infolge gestörter Transkriptionstermination sind auch bei zellulären Stressreaktionen und Krebs bekannt. Diese Entdeckung könnte daher neue therapeutische Strategien inspirieren. Zünftig könnten Medikamente, die gezielt Z-RNAs erzeugen oder deren Erkennung verändern, genutzt werden, um die Immunabwehr zu stärken, Autoimmunerkrankungen zu behandeln, Impfstoffe zu verbessern oder Krebsimmuntherapien zu optimieren – etwa indem sie Tumorzellen zur Selbstzerstörung anregen.
Medizinische Hochschule Hannover
Originalpublikation:
Yin, C., Fedorov, A., Guo, H. et al. Host cell Z-RNAs activate ZBP1 during virus infections. Nature (2025). doi.org/10.1038/s41586-025-09705-5