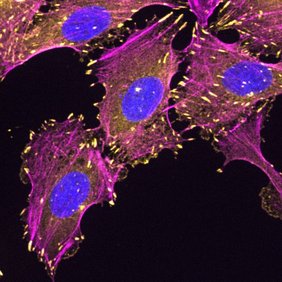
Unser Körper besteht aus geschätzten 32 Billionen einzelnen Zellen. Damit daraus ein zusammenhängendes Ganzes wird, muss der Großteil dieser Zellen fest in seiner Umgebung verankert sein. Für eine solche Verankerung nutzen Körperzellen unter anderem sogenannte fokale Adhäsionen. Diese Strukturen bestehen aus Ansammlungen von Proteinen (=Eiweißen), die zum einen an Moleküle binden, die die Zellen umgeben – und zum anderen im Inneren der Zelle mit dem Skelett der Zelle, dem sogenannten Zytoskelett, verknüpft sind. Bewegt sich eine Zelle beispielsweise während der Wundheilung oder um während der Embryonalentwicklung an ihren Bestimmungsort zu gelangen, müssen sowohl das Zytoskelett als auch die fokalen Adhäsionen dynamisch auf- und wieder abgebaut werden. Findet dies "außer der Reihe" statt, so ist beispielsweise eine Ausbreitung von Tumorzellen die Folge.
Was exakt einen solchen Umbau von Zytoskelett und Adhäsionsstrukturen steuert, ist längst nicht im Detail geklärt. Genau hier setzt eine aktuelle Studie von Forschenden der der Rheinland-Pfälzischen Technischen Universität Kaiserslautern-Landau (RPTU) an: In Kooperation mit der Screening und der Mikroskopie Abteilung des Leibniz-Forschungsinstituts für Molekulare Pharmakologie in Berlin hat ein Team um Professorin Tanja Maritzen mithilfe von kleinen RNA-Molekülen, sogenannten siRNAs, die Herstellung von einzelnen Proteinen unterdrückt – und anschließend beobachtet, wie sich dies jeweils auf die gesamte Zelle auswirkt: „Dazu haben wir die Adhäsionsstrukturen der Zellen angefärbt, mikroskopiert und dann mit automatischer Bildanalyse ausgewertet, ob sie in ihrer Größe oder Anzahl verändert waren“, berichtet Maritzen, die am Fachbereich Biologie der RPTU die Arbeitsgruppe Nanophysiologie leitet.
Insgesamt 18.000 verschiedene Proteine, die in unserem Körper vorkommen, hat das Forschungsteam auf diese Weise unter die Lupe genommen – und ist dabei auf das Stoffwechsel-Enzym Aldolase A aufmerksam geworden, in dessen Abwesenheit die untersuchten Zellen größer waren und mehr fokale Adhäsionen aufwiesen. Auffällig: In den entsprechenden Zellen reicherte sich ein spezieller Zucker an – der wiederum mit einem bestimmten Protein eine Bindung einging. Eine Bindung, die, vereinfacht ausgedrückt, den Startschuss für Wanderbewegungen der Zellen gibt.
Dr. Lennart Hoffmann, Erstautor der Studie, konkretisiert: „Wir haben herausgefunden, dass eine der kleinen Verbindungen, die beim Verstoffwechseln von Zucker entsteht, ein Molekül mit dem komplizierten Namen Fruktose-1,6-Bisphosphat, kurz FBP, nicht nur ein Zwischenprodukt bei der Energiegewinnung aus Zucker ist, sondern auch ein Signal für den Umbau von Zytoskelett und Adhäsionen darstellt.“ Genauer gesagt: FBP sorgt dafür, dass ein Aktivator des Zytoskelettumbaus, ein Protein namens Rac1, nicht länger ausgeschaltet vorliegt. „Das aktive Rac1 führt zur Generierung von neuen Zytoskelett-Elementen an der Zellfront, was eine Ausdehnung der Zellmembran bewirkt – samt gleichzeitiger Verankerung mittels neuer Adhäsionspunkte.“
Schon lange wurde vermutet, dass der Zell-Energiestoffwechsel den Umbau des Zytoskeletts und den Aufbau von Adhäsionsstrukturen beeinflusst: „So wie ein Läufer nicht in unterernährtem Zustand zu einem Rennen starten sollte, ergibt es Sinn, dass eine Zelle Feedback zu ihrem Energiestatus bekommt, bevor sie den energieintensiven Umbau ihres Zytoskeletts in Angriff nimmt“, schlussfolgert Tanja Maritzen.
Die neu gewonnenen Erkenntnisse sind bedeutsam für gleich mehrere Aspekte der Biologie: „Im engeren Sinne für die Bereiche, die sich mit der Adhäsion und Wanderung von Zellen beschäftigen. Sowohl die Wanderung von Immunzellen als auch von metastasierenden Krebszellen könnte durch den von uns aufgedeckten Mechanismus beeinflusst werden“, erklärt Tanja Maritzen mit Blick auf potenzielle Folge-Untersuchungen. Das Zytoskelett spiele aber ebenso bei anderen Prozessen wie der Entstehung neuer Gefäße oder der Insulinsekretion eine Rolle, sodass die Ergebnisse genauso für Forschende, die sich mit diesen Vorgängen beschäftigen, relevant sind.
Technische Universität Kaiserslautern-Landau
Originalpublikation:
Hoffmann, L., Duchmann, M., Lazarow, K. et al. Fructose-1,6-bisphosphate couples glycolytic activity to cell adhesion. Nat Cell Biol (2026). doi.org/10.1038/s41556-026-01911-1