Besonderes Augenmerk haben die Wissenschaftler dabei auf die Krankheit ALS (Amyotrophe Lateralsklerose) gelegt. ALS ist eine bislang unheilbare Erkrankung des zentralen Nervensystems, bei der die Motoneuronen – für die Muskulatur und Bewegung des Körpers zuständige Nervenzellen – zunehmend absterben. Spielen hierbei die Stress-Granuli eine Rolle?
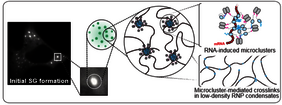
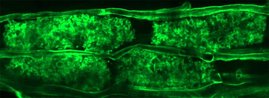
Stress-Granuli bilden sich im Zytoplasma der Zelle und setzen sich aus einer großen Anzahl makromolekularer Komponenten zusammen, u.a. aus Boten-RNAs und RNA-bindenden Eiweißen. Wenn der Stress nachlässt, zerfallen die Granuli normalerweise wieder. Neuere Arbeiten haben jedoch gezeigt, dass sich bei bestimmten Krankheitsbildern die Stress-Granuli in der Zelle nicht auflösen, sondern auch ohne Stress fortbestehen. Dies ist bei ALS der Fall.
“ALS-Patienten leiden an Muskelschwäche und Lähmungserscheinungen. Motorneuronen, die Stress-Granuli beinhalten, degenerieren langsam, was zu einem fortschreitenden Verlust der motorischen Fähigkeiten dieser Patienten führt. Wir müssen die komplexe Biologie der Stress-Granuli besser verstehen, um auf dieser Basis Therapien zu entwickeln, die dem Krankheitsverlauf entgegenwirken. Aber die komplexe Umgebung von Zellen im Organismus macht dies unmöglich”, erklärt Dr. Titus Franzmann, einer der Senior-Autoren der Publikation.
Um ihre Annahmen zur Entstehung der Stress-Granuli zu testen, arbeiteten die Wissenschaftler außerhalb des lebenden Organismus und entwickelten stattdessen im Labor eine kontrollierte Umgebung mit reinsten Komponenten. Sie beobachteten im Reagenzglas, wie sich Stress-Granuli Schritt für Schritt bilden und analysierten die kritischen Faktoren in diesem Prozess.
“Stress-Granuli sind sehr komplexe Gebilde. Trotzdem hängt ihre Entstehung in erster Linie vom Verhalten eines einzigen Eiweißes ab – vom RNA-bindenden Protein G3BP”, sagt Dr. Jordina Guillén-Boixet, eine der Erst-Autorinnen der Studie. “Dieses Protein verändert seine Struktur enorm. Ohne Stress zeigt G3BP einen kompakten Zustand, der die Bildung von Stress-Granuli nicht erlaubt. Aber unter Stress lässt G3BP Bindungen von RNA-Molekülen zu, wodurch das Protein dann auf vielfältige Art interagiert und die Entstehung von Stress-Granuli fördert. Der anschließende Übergang von dynamischen zu nicht-dynamischen Stress-Granuli, zum Beispiel durch anhaltenden Stress, führt vermutlich zum Absterben der Motoneuronen, wie wir es bei der Krankheit ALS beobachten können.“
Das Forschungsprojekt wurde 2015 von der Forschungsgruppe Alberti am BIOTEC der TU Dresden initiiert und geleitet. Ausschlaggebend für den Erfolg war die enge Zusammenarbeit von 23 Wissenschaftlern der TU Dresden, des Max-Planck-Instituts für Molekulare Zellbiologie und Genetik in Dresden, des Europäischen Molekularlabors in Heidelberg und der Washington University in St. Louis (USA). Prof. Simon Alberti: „Viele Fragen sind noch immer offen. Wir werden unser Versuchssystem am BIOTEC weiter intensiv nutzen, um die Suche nach neuen Diagnosemöglichkeiten und Therapien zur Bekämpfung neurodegenerativer Erkrankungen wie ALS zu unterstützen.”
TU Dresden
Originalpublikation:
Jordina Guillén-Boixet, Andrii Kopach, Alex S. Holehouse, Sina Wittmann, Marcus Jahnel, Raimund Schlüßler, Kyoohyun Kim, Irmela R.E.A. Trussina, Jie Wang, Daniel Mateju, Ina Poser, Shovamayee Maharana, Martine Ruer-Gruß, Doris Richter, Xiaojie Zhang, Young-Tae Chang, Jochen Guck, Alf Honigmann, Julia Mahamid, Anthony A. Hyman, Rohit V. Pappu, Simon Alberti, Titus M. Franzmann: „RNA-Induced Conformational Switching and Clustering of G3BP Drive Stress Granule Assembly by Condensation“, Cell 2020
https://doi.org/10.1016/j.cell.2020.03.049